研究意义
本项目面向药品监管过程中的注册审评现代化和智能化需求,致力于提高我国医药行业领域临床试验数据规范化水平、药品信息追溯能力、药品监管审评技术。
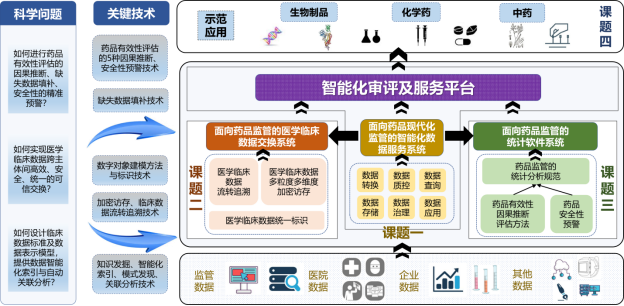
科学问题一
面向临床研究和监管审评的数据表示模型以及智能索引
药品监管需要将临床研究中的数据进行统一描述和标准化转换,从而避免审评过程中出现重复性的数据整理工作,提高药品审评效率。如何设计符合临床数据的数据标准及对应的数据表示模型,并提供经过数据治理的标准化数据智能化索引与自动关联分析是亟待解决的关键科学问题。
科学问题二
面向药品监管需求的医学临床数据跨主体可信交换
药品监管需要在申办方企业、临床试验机构、监管部门等多主体之间交换医学临床数据以实现协同分析,因此面临着来源主体多、安全保障难、协作透明度低等问题。如何面向药品监管需求实现医学临床数据跨主体间高效、安全、统一的可信交换是亟待解决的关键科学问题。
科学问题三
面向药品全生命周期管理中不同场景的针对性的统计理论体系和方法
在药品监管的不同场景中,如何进行药品有效性评估的因果推断、临床缺失数据的填补、药品安全性的精准预警,并针对各种监管业务场景编撰统计分析规范及设计相应的统计软件系统是亟待解决的关键科学问题。
项目主要研究内容
研究内容一
基于医学本体的药品临床研究数据建模与服务平台

研究内容二
基于数字对象的医学临床数据标识和交换技术

研究内容三
面向药品临床研究的统计理论体系与方法

研究内容四
基于药品智能监管平台的临床示范应用
